Publicaties in 2025: de cijfers
De COGEM heeft 76 adviezen en signaleringen uitgebracht in 2025. Dit is ongeveer gelijk aan het gemiddeld aantal publicaties over de afgelopen 5 jaar. Zoals gebruikelijk bestond het leeuwendeel (72) uit adviezen. In 2025 zijn 2 signaleringen en 2 signalerende brieven opgesteld.
De COGEM subcommissie Medisch Veterinair (ScMV) heeft de meeste publicaties (41) voorbereid. De subcommissie Landbouw (ScL) heeft 27 publicaties verzorgd en de subcommissie Ethiek en Maatschappelijke Aspecten (ScEMA) twee. Zes publicaties werden door meerdere subcommissies voorbereid.
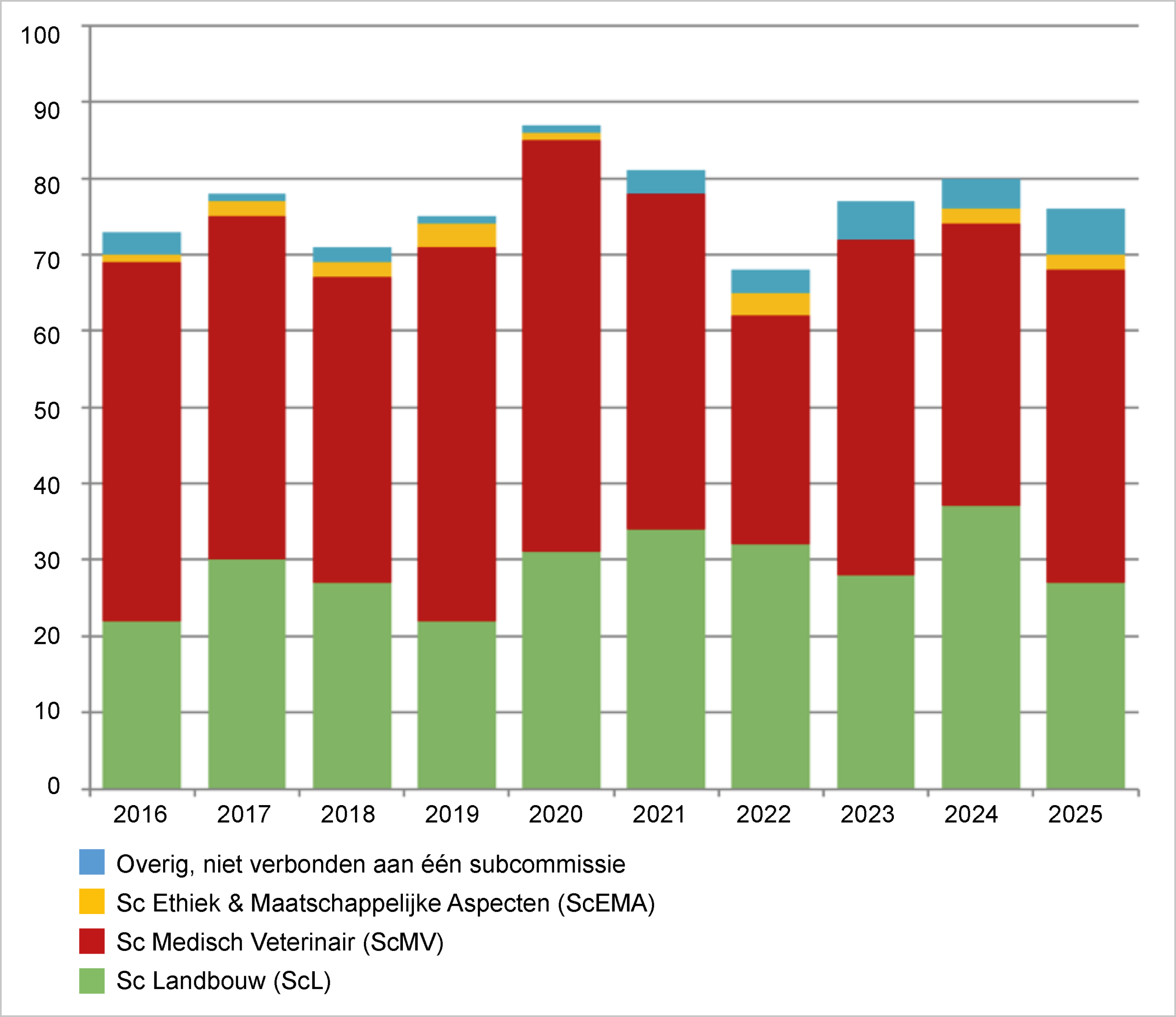
Adviezen
Het merendeel van de publicaties (83%) betrof gevraagde adviezen, voor het merendeel door het Bureau ggo aangevraagd over specifieke vergunningaanvragen. Daarnaast heeft het ministerie van IenW om advies gevraagd over voorstellen om de ggo-regelgeving aan te passen. De ongevraagde adviezen betroffen over het algemeen aanscherpingen en verduidelijkingen van eerdere uitgebrachte adviezen met generieke milieurisicobeoordelingen voor klinische studies en werkzaamheden met virale replicons. Ook is een aantal keren ongevraagd geadviseerd over aanpassing van de Regeling ggo.
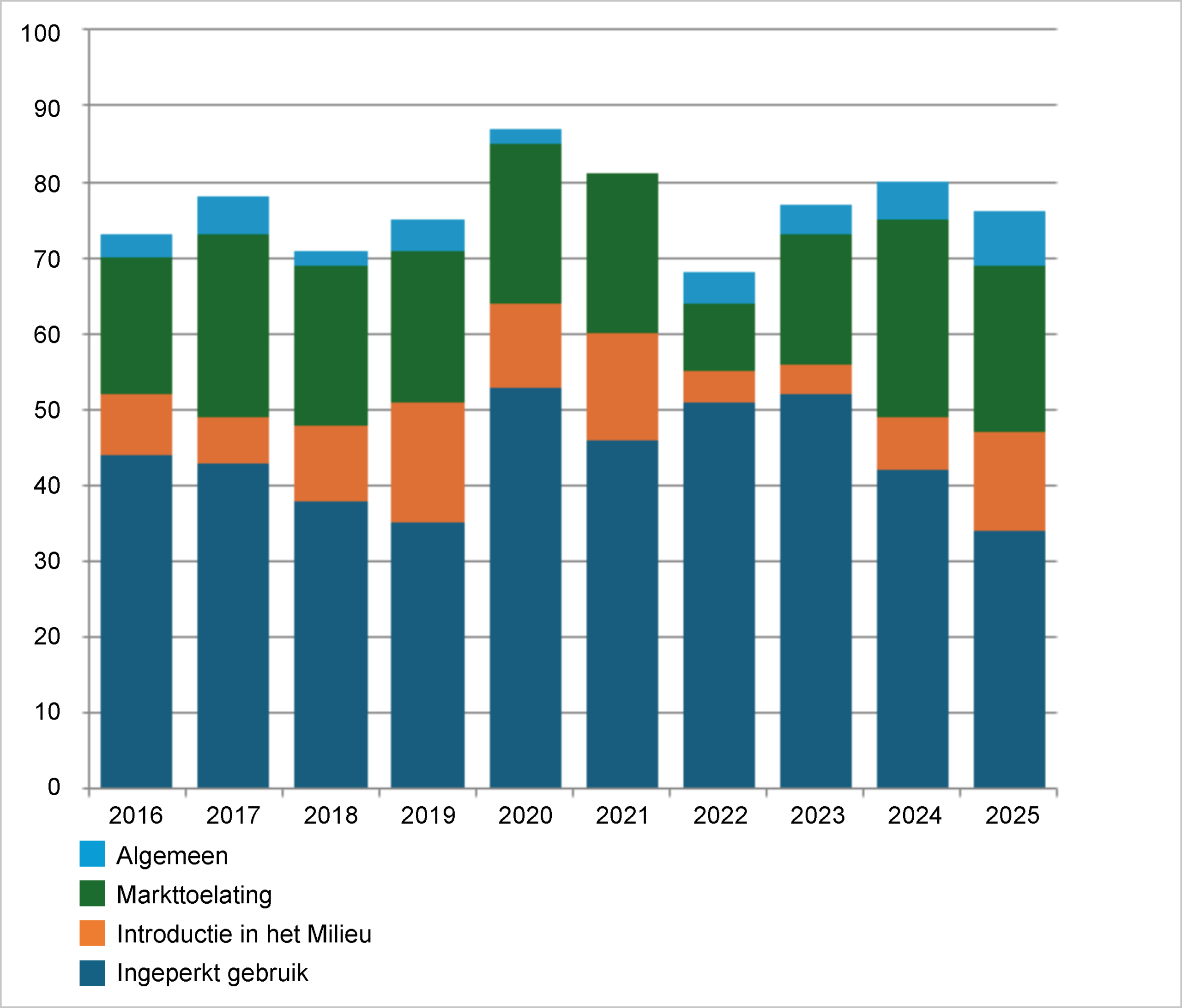
Het aantal adviezen over werkzaamheden onder Ingeperkt Gebruik (IG; experimenten in laboratoria, kassen e.d. ) daalde voor het derde jaar op rij, terwijl het aantal adviezen over Introductie in het Milieu (veldproeven en klinische studies) licht steeg. Dit laatste is terug te voeren tot de grotendeels ongevraagde adviezen over verdere verduidelijking van de eerder uitgevoerde generieke milieurisicobeoordelingen voor klinische studies met ggo’s. Verder is voor het eerst sinds jaren een advies uitgebracht over een veldproef met een genetisch gemodificeerd (gg-)gewas (gg-aardappelen). Het aantal adviezen over marktaanvragen (MA, Europese toelatingen voor vercommercialisering van ggo’s; gentherapieën, gg-vaccins en import van gg-gewassen) blijft al een aantal jaren gelijk.
Signaleringen
In 2025 zijn twee signaleringen uitgebracht. In de eerste signalering is aan de hand van interviews en literatuuronderzoek onderzocht of de dynamiek van het maatschappelijk debat over genetische modificatie in de afgelopen jaren veranderd is. De belangrijkste conclusies van dit onderzoek waren dat er geen breed maatschappelijk debat (meer) is. Het debat is geïnstitutionaliseerd, met stakeholders als deelnemers, en gaat hoofdzakelijk over genetische modificatie in de landbouw. De toon van het debat en de gebruikte argumenten zijn in de loop van de tijd nauwelijks veranderd in dit geïnstitutionaliseerde debat. De dynamiek bleek wel veranderd door de keuze van de Nederlandse overheid om in te stemmen met het voorstel van de Europese Commissie om de zogenoemde NGT1-planten vrij te stellen van de ggo-regelgeving. De stakeholders die kritisch staan ten opzichte van genetische modificatie ervaren de overheid daardoor niet langer als een neutrale partij.
De tweede signalering betrof een gezamenlijke open brief van de Duitse Zentrale Kommission für die Biologische Sicherheit (ZKBS) en de COGEM aan de Europese Commissie. In deze brief uitten beide organisaties hun zorgen over de toelating van geneesmiddelen die zogenoemde self-amplifying mRNA’s (samRNA’s) of virale replicondeeltjes (VRP’s) bevatten. Dit naar aanleiding van de recente markttoelating van een samRNA, zonder dat deze een milieurisicobeoordeling had ondergaan. Beide commissies zijn van mening dat een adequate milieurisicobeoordeling van geneesmiddelen op basis van virale replicons en samRNA’s cruciaal is, zowel om de risico’s te beoordelen alsmede om het vertrouwen en de acceptatie van geneesmiddelen die met behulp van moderne biotechnologie zijn ontwikkeld, te waarborgen. Om deze materie verder te verkennen met onze Europese zusterorganisatie heeft de COGEM eind 2025 een workshop georganiseerd waarin zowel de mogelijkheden, risico’s als de juridische implicaties zijn besproken.
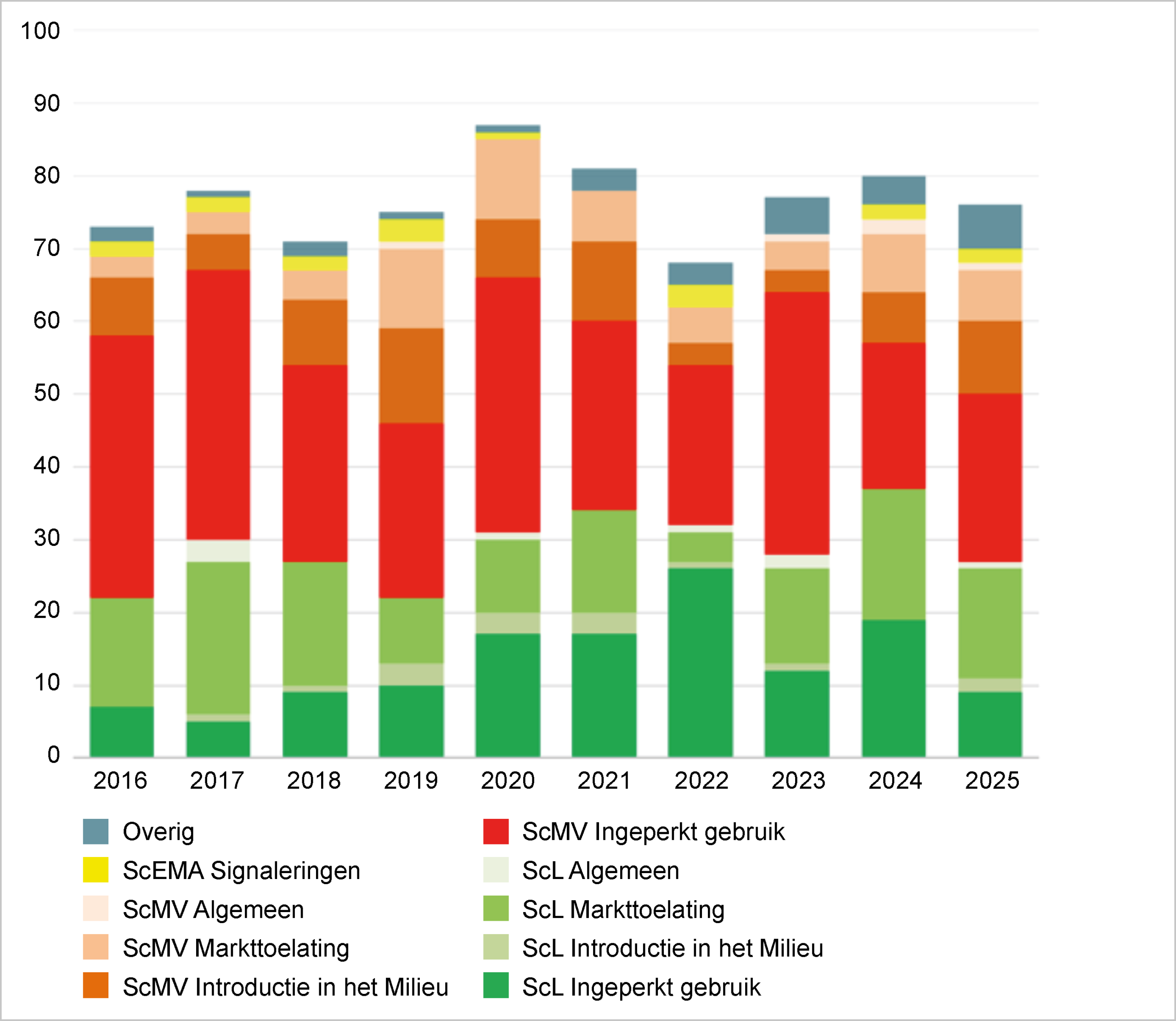
Onderzoeksrapporten
In 2025 zijn drie in opdracht van de COGEM opgestelde onderzoeksrapporten gepubliceerd. Daarnaast zijn een aantal onderzoeksprojecten eind 2025 afgerond die nog niet gepubliceerd zijn Deze onderzoeksrapporten zullen begin 2026 verschijnen. Op de inhoud van de in 2026 gepubliceerde onderzoekrapporten wordt nader ingegaan onder het tabblad Onderzoek.
